Pirofosforna kiselina
Pirofosforna kiselina, još poznata kao difosforna kiselina, je sirupasta tečnost ili viskozna bela čvrsta masa.[2] Pirofosforna kiselina je bezbojna, bezmirisna, higroskopna i rastvorna u vodi, dietil-etru, i etanolu.[3] Dobija se dehidratacijom fosforne kiseline. Pirofosforna kiselina sporo hidrolizuje u prisustvu vode u fosfornu kiselinu.
| Pirofosforna kiselina | |||
|---|---|---|---|
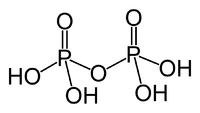
| |||

| |||
| IUPAC ime |
| ||
| Drugi nazivi | difosforna kiselina | ||
| Identifikacija | |||
| CAS registarski broj | 2466-09-3 | ||
| ChemSpider[1] | 996 | ||
| MeSH | |||
| Jmol-3D slike | Slika 1 | ||
| |||
| Svojstva | |||
| Molekulska formula | H4P2O7 | ||
| Molarna masa | 177.98 g/mol | ||
| Tačka topljenja |
61 °C | ||
| Tačka ključanja |
°C | ||
|
| |||
| Infobox references | |||
- 2H3PO4 ⇌ H4P2O7 + H2O
Iako je pirofosforna kiselina četvorobazna, poznate su samo dve vrste njenih soli pirofosfata: sekundarni (npr. Na2H2P2O7) i kvarternarni (npr. Na4P2O7). Soli pirofosforne kiseline imaju velikog značaja u analitičkoj hemiji.[4]
Reference
uredi- ↑ Hettne KM, Williams AJ, van Mulligen EM, Kleinjans J, Tkachenko V, Kors JA. (2010). „Automatic vs. manual curation of a multi-source chemical dictionary: the impact on text mining”. J Cheminform 2 (1): 3. DOI:10.1186/1758-2946-2-3. PMID 20331846.
- ↑ „Material Safety Data Sheet: Pyrophosphoric acid MSDS”. Arhivirano iz originala na datum 2009-04-30. Pristupljeno 2013-04-20.
- ↑ Lide David R., ur. (2006). CRC Handbook of Chemistry and Physics (87th izd.). Boca Raton, FL: CRC Press. 0-8493-0487-3.
- ↑ Neorganska hemija, dr Ilija Rikovski, Građevinska knjiga, Beograd 1983. ISBN 86-395-0237-4