Tioestar
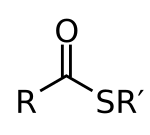
Tioestri su jedinjenja sa funkcionalnom grupom C-S-CO-C. Oni su proizvod esterifikacije karboksilnih kiselina i tiola. Tioestri su široko rasprostranjeni u biohemiji, najpoznatiji derivat je acetil-CoA.
Sinteza uredi
Tioesteri se mogu pripremiti na više načina.[1] Glavni metod pripreme je kondenzacija tiola i karboksilnih kiselina u prisustvu dehidracionog agenta:[2]
- RSH + R'CO2H → RSC(O)R' + H2O
Tipični dehidracioni agens je DCC. Kiselinski anhidridi i neki laktoni takođe reaguju sa tiolima u prisustvu baza.
Oni se takođe formiraju putem karbonilacije alkina i alkena u prisustvu tiola.[3]
Reakcije uredi
Karbonilni centar tioestara je reaktivan. On se reaguje poput blaže verzije kiselinskih hlorida. Tioestri i amini se kombinuju i daju amide:
- R"NH2 + RSC(O)R' → R"2NC(O)R' + RSH
C-H grupa susedna karbonilu tioestara je blago kisela i podleže aldolnoj kondenzaciji. Taj tip reakcije se odvija tokom biosinteze masnih kiselina.
Biohemija uredi
Tioesteri su česti intermedijari mnogih biosintetičkih reakcija, među kojima je formiranje i degradacija masnih kiselina i mevalonata, prekursora steroida. Biosinteza lignina, koji sačinjava veliku frakciju biomase, se odvija putem tioestarskih derivata kafeinske kiseline.[4][5] Neki od njih su malonil-CoA, acetoacetil-CoA, propionil-CoA i cinamoil-CoA. Proces acetogeneze obuhvata formiranje acetil-CoA. Dehidratacioni agens u formiranju ovih tioestara je ATP. Tioestri isto tako učestvuju u obeležavanju proteina ubikvitinom, koji označava proteine za degradaciju.
Izomerna jedinjenja: tionoestri uredi
Tionoestri su izomerni sa tioestrima. Kod tionoestara, sumpor zamenjuje karbonilni kiseonik estara. Metil tionobenzoat je C6H5C(S)OCH3. Takva jedinjenja se tipično pripremaju reakcijom tioacil hlorida sa alkoholom, kao i reakcijom Lovesonovog reagensa sa estrima.[6]
Reference uredi
- ↑ Shin-ichi Fujiwara, Nobuaki Kambe "Thio-, Seleno-, and Telluro-Carboxylic Acid Esters" in Topics in Current Chemistry (2005) volume, 251: pp. 87–140.}{DOI|10.1007/b101007}}
- ↑ Synthesis of thioesters
- ↑ Werner Bertleff, Michael Roeper, Xavier Sava “Carbonylation” Ullmann's Encyclopedia of Industrial Chemistry 2007, Wiley-VCH. DOI: 10.1002/14356007.a05_217.pub2
- ↑ David L. Nelson, Michael M. Cox (2005). Principles of Biochemistry (4th izd.). New York: W. H. Freeman. ISBN 0-7167-4339-6.
- ↑ Donald Voet, Judith G. Voet (2005). Biochemistry (3 izd.). Wiley. ISBN 978-0-471-19350-0.
- ↑ R. J. Cremlyn “An Introduction to Organosulfur Chemistry” John Wiley and Sons: Chichester (1996). ISBN 0-471-95512-4.