Cistin
Cistin je dimerna aminokiselina formirana oksidacijom dva ostatka cisteina koja su kovalentno vezana disulfidnom vezom. Ovo organosumporno jedinjenje ima formulu (SCH2CH(NH2)CO2H)2. Cistin je beli prah, koji se topi na 247-249 °C. Otkrio ga je 1810 Vilijam Hid Volaston. Tek je 1899. bilo pokazano da se cistin može dobiti iz proteina. Te godine je bio izolovan iz goveđih rogova.[4] Putem formiranja disulfidnih veza unutar i između molekula proteina, cistin je značajan determinant tercijarne strukture većine proteina. Na primer, disulfidno vezivanje, zajedno sa vodoničnim vezama i hidrofobnim interakcijama, je parcijalno odgovorno za formiranje glutenske osnove hleba. Ljudska kosa sadrži aproksimativno 5% cistina po masi.[5]
| Cistin | |||
|---|---|---|---|
 |
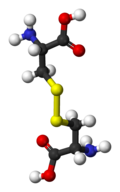 | ||
| Identifikacija | |||
| CAS registarski broj | 56-89-3 | ||
| ChemSpider[1] | 575 | ||
| UNII | 48TCX9A1VT | ||
| KEGG[2] | |||
| ChEMBL[3] | CHEMBL366563 | ||
| Jmol-3D slike | Slika 1 | ||
| |||
| |||
| Svojstva | |||
| Molekulska formula | C6H12N2O4S2 | ||
| Molarna masa | 240.3 g mol−1 | ||
| Opasnost | |||
| Podaci o bezbednosti prilikom rukovanja (MSDS) | External MSDS | ||
|
Ukoliko nije drugačije napomenuto, podaci se odnose na standardno stanje (25 °C, 100 kPa) materijala | |||
| Infobox references | |||
Osobine i nutricioni aspekti uredi
Disulfidna veza se lako redukuje i daje korespondirajući tiol cistein. Ova reakcija je tipično ostvaruje sa tiolima kao što su merkaptoetanol ili ditiotreitol.
- (SCH2CH(NH2)CO2H)2 + 2 RSH → 2 HSCH2CH(NH2)CO2H + RSSR
Iz tog razloga, nutriciona korist i izvori cistina su identični sa cisteinom. Disulfidne veze se otvaraju brže na višim temperaturama.[6].
Vidi još uredi
Reference uredi
- ↑ Hettne KM, Williams AJ, van Mulligen EM, Kleinjans J, Tkachenko V, Kors JA. (2010). „Automatic vs. manual curation of a multi-source chemical dictionary: the impact on text mining”. J Cheminform 2 (1): 3. DOI:10.1186/1758-2946-2-3. PMID 20331846.
- ↑ Joanne Wixon, Douglas Kell (2000). „Website Review: The Kyoto Encyclopedia of Genes and Genomes — KEGG”. Yeast 17 (1): 48–55. DOI:10.1002/(SICI)1097-0061(200004)17:1<48::AID-YEA2>3.0.CO;2-H.
- ↑ Gaulton A, Bellis LJ, Bento AP, Chambers J, Davies M, Hersey A, Light Y, McGlinchey S, Michalovich D, Al-Lazikani B, Overington JP. (2012). „ChEMBL: a large-scale bioactivity database for drug discovery”. Nucleic Acids Res 40 (Database issue): D1100-7. DOI:10.1093/nar/gkr777. PMID 21948594.
- ↑ „Cystine”. Encyclopædia Britannica. 2007.
- ↑ Gortner, R. A.; W. F. Hoffman, W. F. (1941), „l-Cystine”, Organic Syntheses; Coll. Vol. 1: 194
- ↑ M.A. Aslaksena, O.H. Romarheima, T. Storebakkena and A. Skrede (2006-06-28). „Evaluation of content and digestibility of disulfide bonds and free thiols in unextruded and extruded diets containing fish meal and soybean protein sources”. Animal Feed Science and Technology 128 (3-4): 320–330. DOI:10.1016/j.anifeedsci.2005.11.008.
Literatura uredi
- „Cystine”. Encyclopædia Britannica. 2007.