Kalijum sulfat
Kalijum-sulfat je neorgansko hemijsko jedinjenje hemijske formule K2SO4.
| Kalijum-sulfat | |||
|---|---|---|---|
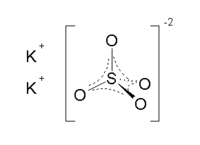
| |||
| Drugi nazivi | Potašum-sulfat | ||
| Identifikacija | |||
| CAS registarski broj | 7778-80-5 | ||
| PubChem[1][2] | 24507 | ||
| ChemSpider[3] | 22915 | ||
| UNII | 1K573LC5TV | ||
| KEGG[4] | |||
| MeSH | |||
| ChEBI | 32036 | ||
| ChEMBL[5] | CHEMBL1201793 | ||
| RTECS registarski broj toksičnosti | TT5900000 | ||
| Jmol-3D slike | Slika 1 | ||
| |||
| |||
| Svojstva | |||
| Molarna masa | 174.259 g/mol (anhidrid) | ||
| Agregatno stanje | Bela kristalna supstanca | ||
| Gustina | 2.66 g/cm3, anhidrovan | ||
| Rastvorljivost u vodi | 11.1 g/100 ml (20 °C) | ||
| Struktura | |||
| Kristalna rešetka/struktura | ortorombična | ||
| Opasnost | |||
| Podaci o bezbednosti prilikom rukovanja (MSDS) | External MSDS | ||
| Opasnost u toku rada | Iritant | ||
| R i S-oznake | nema | ||
| Srodna jedinjenja | |||
| Drugi anjoni | Kalijum-hidrogensulfat Kalijum-sulfit Kalijum-bisulfit Kalijum-persulfat | ||
| Drugi katjoni | Litijum-sulfat Natrijum-sulfat Magnezijum-sulfat | ||
|
| |||
| Infobox references | |||
Rasprostranjenost u prirodi uredi
Javlja se u velikim količinama u raznim dvogubim solima u štasfurtskim naslagama, kao što su šenit i kainit, koji i služe za dobijanje kalijum-sulfata.[6]
Dobijanje uredi
Šenit se odvaja hlađenjem iz vrućeg zasićenog rastvora kainita, a potom tretira rastvorom kalijum-hlorida:
- K2SO4 • MgSO4 • 6H2O + 2KCl → 2K2SO4 + MgCl2 + 6H2O
Prvo se dobija slabo rastvoran, anhidrovani kalijum-sulfat, a koncentrovanjem se iz filtrata taloži karnalit iz koga se dobijaju kalijum-hlorid i magnezijum-hlorid.[6]
Kalijum-sulfat se još može dobiti zagrevanjem kalijum-hlorida sa sumpornom kiselinom, ali u manjim količinama, a inače je sporedni proizvod pri dobijanju kalijum-dihromata i kalijum-permanganata.[6]
Svojstva uredi
To je supstanca koju čine bezbojni kristali bez vode. U vodi se slabo rastvara (na 0 °C 6,85 g u 100 g vode).[6]
Upotreba uredi
Koristi se za pravljenje kalijumove stipse i kao veštačko đubrivo, posebno prilikom gajenja duvana i pšenice. Osim kalijum-sulfata, kao đubrivo se koristi i kalijum-hlorid, ali kod paradajza, luka, pasulja i bostana prednost se daje kalijum-sulfatu jer su pomenute biljke osetljive na veće koncentracije hlora.[6]
Izvori uredi
- ↑ Li Q, Cheng T, Wang Y, Bryant SH (2010). „PubChem as a public resource for drug discovery.”. Drug Discov Today 15 (23-24): 1052-7. DOI:10.1016/j.drudis.2010.10.003. PMID 20970519.
- ↑ Evan E. Bolton, Yanli Wang, Paul A. Thiessen, Stephen H. Bryant (2008). „Chapter 12 PubChem: Integrated Platform of Small Molecules and Biological Activities”. Annual Reports in Computational Chemistry 4: 217-241. DOI:10.1016/S1574-1400(08)00012-1.
- ↑ Hettne KM, Williams AJ, van Mulligen EM, Kleinjans J, Tkachenko V, Kors JA. (2010). „Automatic vs. manual curation of a multi-source chemical dictionary: the impact on text mining”. J Cheminform 2 (1): 3. DOI:10.1186/1758-2946-2-3. PMID 20331846.
- ↑ Joanne Wixon, Douglas Kell (2000). „Website Review: The Kyoto Encyclopedia of Genes and Genomes — KEGG”. Yeast 17 (1): 48–55. DOI:10.1002/(SICI)1097-0061(200004)17:1<48::AID-YEA2>3.0.CO;2-H.
- ↑ Gaulton A, Bellis LJ, Bento AP, Chambers J, Davies M, Hersey A, Light Y, McGlinchey S, Michalovich D, Al-Lazikani B, Overington JP. (2012). „ChEMBL: a large-scale bioactivity database for drug discovery”. Nucleic Acids Res 40 (Database issue): D1100-7. DOI:10.1093/nar/gkr777. PMID 21948594.
- ↑ 6,0 6,1 6,2 6,3 6,4 Parkes, G. D. & Fil, D. 1973. Melorova moderna neorganska hemija. Naučna knjiga. Beograd.