Hipofosforasta kiselina
Hipofosforasta kiselina je fosforova kiseonična kiselina i vrlo jako redukciono sredstvo formule H3PO2. Neorganski hemičari ovu kiselinu zovu upravo tako (takođe „HPK") iako je IUPAC-ovo ime dihidridohidroksidooksidofosfor ili samo fosfinska kiselina. Ona je bezbojno jedinjenje koje se brzo topi, rastvara u vodi, dioksanu i alkoholima. Formula za hipofosforastu kiselinu je obično H3PO2 ali malo detaljniji zapis bi bio HOP(O)H2 koji pokazuje jednobazni karakter. Soli ove kiseline su fosfinati (hipofosfiti).[5][6]
| Hipofosforasta kiselina | |||
|---|---|---|---|

| |||
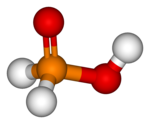
| |||
| IUPAC ime |
| ||
| Identifikacija | |||
| CAS registarski broj | 6303-21-5 | ||
| PubChem[1][2] | 3085127 (2H3) | ||
| ChemSpider[3] | 10449263 | ||
| UN broj | UN 3264 | ||
| KEGG[4] | |||
| MeSH | |||
| ChEBI | 29031 | ||
| Jmol-3D slike | Slika 1 | ||
| |||
| |||
| Svojstva | |||
| Molekulska formula | H3PO2 | ||
| Molarna masa | 66.00 g/mol | ||
| Gustina | 1.274 g/cm3, tečnost | ||
| Tačka topljenja |
26.5 °C (299,5 K) | ||
| Tačka ključanja |
106 °C (379 K) decomp. | ||
| Rastvorljivost u vodi | pomešljiva | ||
| pKa | 1.2 | ||
| Struktura | |||
| Oblik molekula (orbitale i hibridizacija) | pseudo-tetraedarna | ||
| Opasnost | |||
| Podaci o bezbednosti prilikom rukovanja (MSDS) | JT Baker | ||
| EU-klasifikacija | not listed | ||
| Srodna jedinjenja | |||
| Srodna kiseonične kiseline | Fosforasta kiselina Fosforna kiselina Metafosforna kiselina Pirofosforna kiselina | ||
| Сродна једињења | Natrijum-hipofosfit Barijum-hipofosfit | ||
|
| |||
| Infobox references | |||
HOP(O)H2 postoji zajedno sa manjim tautomerom HP(OH)2. Ponekad je taj tautomer tumačen kao hipofosforasta kiselina a glavni kao fosfinska kiselina.
Inače, hipofosforastoj kiselini pripada anhidrid fosfor(III)-oksid. Glavna kiselina u ovoj grupi je fosforasta kiselina.
Dobijanje uredi
Industrijski, ova kiselina se dobija u dva koraka. Hipofosfiti alkalnih metala i zemnoalkalnih metala se dobijaju delovanjem fosfora sa rastvorom određenog hidroksida, npr. Ca(OH)2.
- P4 + 3OH− + 3H2O → 3H2PO2− + PH3
Čista kiselina se priprema delovanjem jakih kiselina na hipofosfitne soli.
- H2PO2− + H+ → H3PO2
Alternativno, H3PO2 se dobija oksidacijom fosfina sa jodom u vodi.
- PH3 + 2I2 + 2H2O → H3PO2 + 4I− + 4H+
Hipofosforasta kiselina je obično dostupna u obliku 50% rastvora.
Primena uredi
Hipofosforasta kiselina se koristi u pravljenju farmaceutskih proizvoda, obezbojavanju polimera i u dobijanju plemenitih ili negvozdenih metala. Glavna upotreba joj je u neelektronom popločavanju. Drugim rečima, u izbacivanju odabranih metalnih premaza na osetljivim površinama. U organskoj hemiji, H3PO2 je najbolje znana po redukciji diazonijumskih soli pretvaranjem ArN2+ u Ar-H.[7][8] Kada je u diazotovanom koncentrovanom rastvoru hipofosforaste kiseline aminski supstituent, on se može ukloniti iz arena, uglavnom alkil-arena.
Neorganski i organski derivati uredi
Razni derivati su poznati kod dva vodonikova atoma direktno vezana za fosfor jer mogu biti zamenjeni raznim organskim grupama. Ovi derivati su poznati pod nazivom fosfinskih kiselina a njihove soli pod nazivom fosfinata. Na primer, formaldehid i H3PO2 reaguju da bi dali (HOCH2)2PO2H. Proizvod reakcije je srodan onom kod dodavanja tiola i HCN aldehidima. Slično tome, dodaje se na Majklove primaoce, npr. sa akrilamidom daje H(HO)P(O)CH2CH2C(O)NH2.
Par kompleksa metala su nastali od H3PO2 a jedan primer je Ni(O2PH2)2.
Reference uredi
- ↑ Li Q, Cheng T, Wang Y, Bryant SH (2010). „PubChem as a public resource for drug discovery.”. Drug Discov Today 15 (23-24): 1052-7. DOI:10.1016/j.drudis.2010.10.003. PMID 20970519.
- ↑ Evan E. Bolton, Yanli Wang, Paul A. Thiessen, Stephen H. Bryant (2008). „Chapter 12 PubChem: Integrated Platform of Small Molecules and Biological Activities”. Annual Reports in Computational Chemistry 4: 217-241. DOI:10.1016/S1574-1400(08)00012-1.
- ↑ Hettne KM, Williams AJ, van Mulligen EM, Kleinjans J, Tkachenko V, Kors JA. (2010). „Automatic vs. manual curation of a multi-source chemical dictionary: the impact on text mining”. J Cheminform 2 (1): 3. DOI:10.1186/1758-2946-2-3. PMID 20331846.
- ↑ Joanne Wixon, Douglas Kell (2000). „Website Review: The Kyoto Encyclopedia of Genes and Genomes — KEGG”. Yeast 17 (1): 48–55. DOI:10.1002/(SICI)1097-0061(200004)17:1<48::AID-YEA2>3.0.CO;2-H.
- ↑ Lide David R., ur. (2006). CRC Handbook of Chemistry and Physics (87th izd.). Boca Raton, FL: CRC Press. 0-8493-0487-3.
- ↑ Susan Budavari, ur. (2001). The Merck Index: An Encyclopedia of Chemicals, Drugs, and Biologicals (13th izd.). Merck Publishing. ISBN 0-911910-13-1.
- ↑ Robison, M. M.; Robison, B. L. (1956). "2,4,6-Tribromobenzoic acid". Org. Synth. 36:94; Coll. Vol. 4:947.
- ↑ Kornblum, N. (1941). "3,3'-Dimethoxybiphenyl and 3,3'-dimethylbiphenyl". Org. Synth. 21:30; Coll. Vol. 3:295.
Literatura uredi
- ChemicalLand21 Listing Arhivirano 2013-01-02 na Archive.is-u
- D. E. C. Corbridge "Phosphorus: An Outline of its Chemistry, Biochemistry, and Technology" 5th Edition Elsevier: Amsterdam. ISBN 0-444-89307-5.
- V. V. Popik, A. G. Wright, T. A. Khan, J. A. Murphy "Hypophosphorous Acid" in Encyclopedia of Reagents for Organic Synthesis (Ed: L. Paquette) 2004, J. Wiley & Sons, New York. DOI: 10.1002/047084289.
- D.W.Rich, M.C. Smith, Electroless Deposition of Nickel, Cobalt & Iron. IBM Corporation, Poughkeepsie, NY(1971)