Dimetilacetamid
Dimetilacetamid (DMA) je organsko jedinjenje sa formulom CH3C(O)N(CH3)2. Ovo bezbojno jedinjenje se meša sa vodom. Ono ima visoku tačku ključanja. Koristi se kao polarni rastvarač u organskoj sintezi. DMA se meša sa većinom drugih rastvarača, mada je slabo rastvoran u alifatičnim ugljovodonicima.
| Dimetilacetamid | |||
|---|---|---|---|
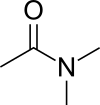
| |||

| |||
| IUPAC ime |
| ||
| Identifikacija | |||
| Abrevijacija | DMAc[2] | ||
| CAS registarski broj | 127-19-5 | ||
| PubChem[3][4] | 31374 | ||
| ChemSpider[5] | 29107 | ||
| UNII | JCV5VDB3HY | ||
| EINECS broj | |||
| MeSH | |||
| ChEMBL[6] | CHEMBL11873 | ||
| RTECS registarski broj toksičnosti | AB7700000 | ||
| Bajlštajn | 1737614 | ||
| Jmol-3D slike | Slika 1 Slika 2 | ||
| |||
| |||
| Svojstva | |||
| Molekulska formula | C4H9NO | ||
| Molarna masa | 87.12 g mol−1 | ||
| Agregatno stanje | Bezbona tečnost | ||
| Miris | Amoniacal | ||
| Gustina | 937 mg mL−1 | ||
| Tačka topljenja |
-20 °C, 253 K, -4 °F | ||
| Tačka ključanja |
165 °C, 438.2 K, 329 °F | ||
| Rastvorljivost u vodi | Meša se | ||
| log P | −0,253 | ||
| Napon pare | 300 Pa | ||
| λmax | 270 nm | ||
| Apsorbancija | 1,00 | ||
| Indeks prelamanja (nD) | 1,4375 | ||
| Viskoznost | 1,956 mPa s | ||
| Termohemija | |||
| Standardna entalpija stvaranja jedinjenja ΔfH |
−300,1 kJ mol−1 | ||
| Std entalpija sagorevanja ΔcH |
−2,5835–−2.5805 MJ mol−1 | ||
| Specifični toplotni kapacitet, C | 178,2 J K−1 mol−1 | ||
| Opasnost | |||
| EU-klasifikacija | |||
| EU-indeks | 616-011-00-4 | ||
| NFPA 704 | |||
| R-oznake | R61, R20/21 | ||
| S-oznake | S45 | ||
| Tačka paljenja | 63 °C | ||
| Tačka spontanog paljenja | 490 °C | ||
| Eksplozivni limiti | 1,8–11,5% | ||
| LD50 |
| ||
| Srodna jedinjenja | |||
| Srodna jedinjenja | |||
|
Ukoliko nije drugačije napomenuto, podaci se odnose na standardno stanje (25 °C, 100 kPa) materijala | |||
| Infobox references | |||
Sinteza, reakcije, primena uredi
DMA se priprema reakcijom dimetilamina sa anhidridom sirćetne kiseline i estrima sirćetne kiseline. Dehidracija soli dimetilamina i sirćetne kiseline je alternativni sintetički put:[7]
- CH3CO2-N(CH3)2H2 → H2O + CH3CON(CH3)2
Hemijske reakcije dimetilacetamida su tipične za N,N-disupstituisane amide. On se hidroluje u prisustvu kiselina:
- CH3CON(CH3)2 + H2O + HCl → CH3COOH + (CH3)2NH2+Cl-
On je otporan na baze. Iz tog razloga je DMA koristan rastvarač za reakcije u kojima učestvuju jake baze poput natrijum hidroksida.[8]
Reference uredi
- ↑ „dimethylacetamide - Compound Summary”. PubChem Compound. USA: National Center for Biotechnology Information. 26. 3. 2005.. Identification. Pristupljeno 19. 4. 2012.
- ↑ Munro, D. D.; Stoughto, R. B. (1965). „Dimethylacetamide (DMAC) and Dimethylformamide (DMFA). Effect on Percutaneous Absorption”. Archives of Dermatology 92 (5): 585–586. DOI:10.1001/archderm.1965.01600170101020. PMID 5844405.
- ↑ Li Q, Cheng T, Wang Y, Bryant SH (2010). „PubChem as a public resource for drug discovery.”. Drug Discov Today 15 (23-24): 1052-7. DOI:10.1016/j.drudis.2010.10.003. PMID 20970519.
- ↑ Evan E. Bolton, Yanli Wang, Paul A. Thiessen, Stephen H. Bryant (2008). „Chapter 12 PubChem: Integrated Platform of Small Molecules and Biological Activities”. Annual Reports in Computational Chemistry 4: 217-241. DOI:10.1016/S1574-1400(08)00012-1.
- ↑ Hettne KM, Williams AJ, van Mulligen EM, Kleinjans J, Tkachenko V, Kors JA. (2010). „Automatic vs. manual curation of a multi-source chemical dictionary: the impact on text mining”. J Cheminform 2 (1): 3. DOI:10.1186/1758-2946-2-3. PMID 20331846.
- ↑ Gaulton A, Bellis LJ, Bento AP, Chambers J, Davies M, Hersey A, Light Y, McGlinchey S, Michalovich D, Al-Lazikani B, Overington JP. (2012). „ChEMBL: a large-scale bioactivity database for drug discovery”. Nucleic Acids Res 40 (Database issue): D1100-7. DOI:10.1093/nar/gkr777. PMID 21948594.
- ↑ Cheung, H.; Tanke, R. S.; Torrence, G. P. (2005). „Acetic Acid”. Ullmann’s Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. DOI:10.1002/14356007.a01_045.pub2.
- ↑ Zen, S.; Kaji, E. (1977), „Dimethyl nitrosuccinate”, Organic Syntheses 57: 60; Coll. Vol. 6: 503
