Kinurenska kiselina
Kinurenska kiselina (transtorin, KYNA) je proizvod normalnog metabolizma aminokiseline L-triptofan. Za kinurensku kiselinu je bilo pokazano da poseduje neuro-aktivna svojstva. Ona deluje kao antiepileptik, najverovatnije putem delovanja kao antagonist na pobuđivačkim aminokiselinskim receptorima. Ona može da utiče na važne neurofiziološke i neuropatološke procese. Kao rezultat toga, kinurenska kiselina je bila razmatrana za primjenu u terapiji određenih neurobioloških poremećaja. U kontrastu s tim, povišeni nivoi kinurenske kiseline su bili su povezani sa pojedinim patološkim stanjima.
| Kinurenska kiselina | |||
|---|---|---|---|
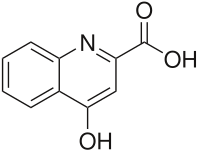
| |||
| IUPAC ime |
| ||
| Drugi nazivi | Transtorin | ||
| Identifikacija | |||
| CAS registarski broj | 492-27-3 | ||
| PubChem[1][2] | 3845 | ||
| ChemSpider[3] | 3712 | ||
| KEGG[4] | |||
| ChEMBL[5] | CHEMBL299155 | ||
| Jmol-3D slike | Slika 1 | ||
| |||
| |||
| Svojstva | |||
| Molekulska formula | C10H7N1O3 | ||
| Molarna masa | 189.168 g/mol | ||
| Tačka topljenja |
282.5 °C | ||
|
Ukoliko nije drugačije napomenuto, podaci se odnose na standardno stanje (25 °C, 100 kPa) materijala | |||
| Infobox references | |||
Kinurensku kiselinu je otkrio nemački hemičar Justus fon Libig 1853. u urinu pasa.[6]
Ona se formira iz L-kinurenina reakcijom koja je katalizovana enzimom kinurenin—oksoglutarat transaminaza.
Mehanizam akcije uredi
Za transtorin je utvrđeno da deluje na tri receptora:
- Kao nekompetitivni antagonist glicinskog mesta NMDA receptora.
- Antagonist α7 nikotin acetilholinskog receptora. Ovo dejstvo je suprotno jednom drugom metabolitu triptofana, 5-hidroksi indolsirćetnoj kiselini.[7]
- Ligand orfanskog G protein-spregnutog receptora GPR35.[8]
Literatura uredi
- ↑ Li Q, Cheng T, Wang Y, Bryant SH (2010). „PubChem as a public resource for drug discovery.”. Drug Discov Today 15 (23-24): 1052-7. DOI:10.1016/j.drudis.2010.10.003. PMID 20970519.
- ↑ Evan E. Bolton, Yanli Wang, Paul A. Thiessen, Stephen H. Bryant (2008). „Chapter 12 PubChem: Integrated Platform of Small Molecules and Biological Activities”. Annual Reports in Computational Chemistry 4: 217-241. DOI:10.1016/S1574-1400(08)00012-1.
- ↑ Hettne KM, Williams AJ, van Mulligen EM, Kleinjans J, Tkachenko V, Kors JA. (2010). „Automatic vs. manual curation of a multi-source chemical dictionary: the impact on text mining”. J Cheminform 2 (1): 3. DOI:10.1186/1758-2946-2-3. PMID 20331846.
- ↑ Joanne Wixon, Douglas Kell (2000). „Website Review: The Kyoto Encyclopedia of Genes and Genomes — KEGG”. Yeast 17 (1): 48–55. DOI:10.1002/(SICI)1097-0061(200004)17:1<48::AID-YEA2>3.0.CO;2-H.
- ↑ Gaulton A, Bellis LJ, Bento AP, Chambers J, Davies M, Hersey A, Light Y, McGlinchey S, Michalovich D, Al-Lazikani B, Overington JP. (2012). „ChEMBL: a large-scale bioactivity database for drug discovery”. Nucleic Acids Res 40 (Database issue): D1100-7. DOI:10.1093/nar/gkr777. PMID 21948594.
- ↑ Liebig, J., Uber Kynurensäure, Justus Liebigs Ann. Chem., 86: 125-126, 1853.
- ↑ Grilli M, Raiteri L, Patti L, Parodi M, Robino F, Raiteri M, Marchi M (2006). „Modulation of the function of presynaptic alpha7 and non-alpha7 nicotinic receptors by the tryptophan metabolites, 5-hydroxyindole and kynurenate in mouse brain”. Br. J. Pharmacol. 149 (6): 724–32. DOI:10.1038/sj.bjp.0706914. PMC 2014664. PMID 17016503.
- ↑ Wang J, Simonavicius N, Wu X, Swaminath G, Reagan J, Tian H, Ling L (2006). „Kynurenic acid as a ligand for orphan G protein-coupled receptor GPR35”. J. Biol. Chem. 281 (31): 22021–8. DOI:10.1074/jbc.M603503200. PMID 16754668.