Disulfidna veza
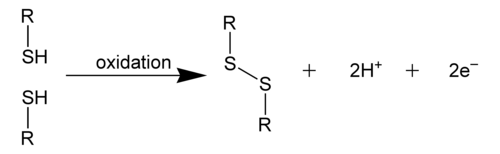
Disulfidna veza je kovalentna veza, obično nastaje spajanjem dve tiolne grupe.[1] Ovaj link se takođe naziva SS-veza ili disulfidni most. Ukupna povezanost je dakle R-S-S-R. Ova terminologija je u širokoj upotrebi u biohemiji. Nekad se ova veza nazivala persulfid, po analogiji sa kongenernim peroksidom (R-O-O-R), ali je ta terminologija nezastupljena.
Osobine uredi
Disulfidna veza je jaka. Njena tipična energija disocijacije veze je 60 kcal/mol. Ona je oko 40% slabija od C-C i C-H veza, i stoga se disulfidna veza često naziva "slabim linkom" u mnogim molekulima. Osim toga, odražavajući polarizabilnost dvovalentnig sumpora, S-S veza je podložna cijepanju polarnim reagensima elektrofilima a posebno nukleofilima.[2]
- RS-SR + Nu- → RS-Nu + RS-
Disulfidna veza je oko 2.05 Å dugačka, što je 0.5 Å duže od C-C veze. Rotacija oko S-S ose ima nisku barijeru. Disulfidi pokazuju izrazitu sklonost za diedralne uglove koji se približavaju uglu od 90 °. Kada je ugao blizo 0 ° ili 180 °, disulfid je znatno bolji oksidacioni agens.
Disulfidi sa dve iste R grupe su simetrični. Primeri takvih jedinjenja su difenil disulfid i dimetil disulfid. Asimetrični disulfidi imaju dve različite R grupe.[3]
Iako hidrogenacija disulfida obično nije praktična, konstanta ravnoteže ove reakcije može da služi kao mera standardnog redoks potencijala disulfida:
- RSSR + H2 → 2 RSH
Ova vrednost je oko -250 mV (pH = 7). U poređenju s tim, standardni redukcini potencijal ferodoksina ja oko -430 mV.
Reference uredi
- ↑ Donald Voet, Judith G. Voet (2005). Biochemistry (3 izd.). Wiley. ISBN 978-0-471-19350-0.
- ↑ Cremlyn, R. J. W. (1996). An introduction to organosulfur chemistry. New York: Wiley. ISBN 0-471-95512-4.
- ↑ Sevier, C. S. and Kaiser, C. A. (2002). „Formation and transfer of disulphide bonds in living cells”. Nature Reviews Molecular and Cellular Biology 3 (11): 836–847. DOI:10.1038/nrm954. PMID 12415301.
Literatura uredi
- Sela M, Lifson S. (1959). „The reformation of disulfide bridges in proteins”. Biochim Biophys Acta 36 (2): 471–8. DOI:10.1016/0006-3002(59)90188-X. PMID 14444674.
- Stark GR.; Stern, K; Atala, A; Yoo, J (1977). „Cleavage at cysteine after cyanylation”. Methods Enzymol 47: 129–32. DOI:10.1016/j.ymeth.2008.09.005. PMID 927170.
- Thornton JM. (1981). „Disulphide bridges in globular proteins”. J Mol Biol 151 (2): 261–87. DOI:10.1016/0022-2836(81)90515-5. PMID 7338898.
- Thannhauser TW, Konishi Y, Scheraga HA. (1984). „Sensitive quantitative analysis of disulfide bonds in polypeptides and proteins”. Anal Biochem 138 (1): 181–8. DOI:10.1016/0003-2697(84)90786-3. PMID 6547275.
- Wu J, Watson JT. (1998). „Optimization of the cleavage reaction for cyanylated cysteinyl proteins for efficient and simplified mass mapping”. Anal Biochem 258 (2): 268–76. DOI:10.1006/abio.1998.2596. PMID 9570840.
- Futami J, Tada H, Seno M, Ishikami S, Yamada H. (2000). „Stabilization of human RNase 1 by introduction of a disulfide bond between residues 4 and 118”. J Biochem 128 (2): 245–50. PMID 10920260.
- Wittenberg, G, Danon, A (2008). „Disulfide bond formation in chloroplasts: Formation of disulfide bonds in signaling chloroplast proteins”. Plant Science 175 (4): 459–466. DOI:10.1016/j.plantsci.2008.05.011.
- Kadokura, Hiroshi; Katzen, Federico; Beckwith, Jon (2003). „Protein Disulfide Bond Formation in Prokaryotes”. Annual Review of Biochemistry 72: 111. DOI:10.1146/annurev.biochem.72.121801.161459. PMID 12524212.
- Tu, B. P.; Weissman, JS (2004). „Oxidative protein folding in eukaryotes: mechanisms and consequences”. The Journal of Cell Biology 164 (3): 341. DOI:10.1083/jcb.200311055. PMC 2172237. PMID 14757749.
- Ellgaard, Lars; Ruddock, Lloyd W. (2005). „The human protein disulphide isomerase family: substrate interactions and functional properties”. EMBO reports 6 (1): 28. DOI:10.1038/sj.embor.7400311. PMC 1299221. PMID 15643448.
- Cremlyn, R. J. W. (1996). An introduction to organosulfur chemistry. New York: Wiley.